"Heureka!" (3)
| 28. Oktober 2014
Mit dem DNA-Synthesizer werden vollautomatisch Oligonukleotide für verschiedene Anwendungen hergestellt. (Foto: Johannes Winkler)
Die erfolgreiche Behandlung von Erkrankungen wie Krebs erfordert besonders effiziente Arzneimittel. Forscher am Department für Pharmazeutische Chemie der Universität Wien haben nicht nur neue vielversprechende Wirkstoffe entdeckt, sondern auch verbesserte Methoden zu ihrer Herstellung entwickelt.
uni:view: Herr Winkler, Sie haben gemeinsam mit Ihren Kollegen Christian Noe, Mehrdad  Dirin, Bodo Lachmann und Ernst Urban am Department für Pharmazeutische Chemie der Fakultät für Lebenswissenschaften etwas erfunden, das die Zukunft der Arzneimittelbehandlung entscheidend verändern könnte. Worum handelt es sich genau?
Dirin, Bodo Lachmann und Ernst Urban am Department für Pharmazeutische Chemie der Fakultät für Lebenswissenschaften etwas erfunden, das die Zukunft der Arzneimittelbehandlung entscheidend verändern könnte. Worum handelt es sich genau?
Johannes Winkler: Bei unserer Erfindung handelt es sich um eine Patenteinreichung, die neue Wirkstoffe aus der Klasse der Oligonukleotide und eine verbesserte Methode zur Herstellung dieser – aber auch ähnlicher Substanzen – umfasst. Oligonukleotide sind kurze, rein synthetische Nukleinsäuresequenzen, die als Antisense oder siRNA-Moleküle, aber auch für andere Anwendungen verwendet werden können.
uni:view: Was ist das Besondere an diesen neuen Wirkstoffen und welches Anwendungspotenzial sehen Sie dafür?
Winkler: Therapeutische Oligonukleotide sind eine enorm vielversprechende Klasse neuer Wirkstoffe, die direkt auf genomischer Ebene wirken und einige wichtige Vorteile haben. Damit ergeben sich neue Möglichkeiten der Pharmakotherapie von vielen Erkrankungen, unter anderem Virusinfektionen und Krebs. So ist es etwa möglich, rein auf der Basis der Gensequenz – also der Abfolge der Nukleinbasen A, C, G, und T – jedes beliebige Genprodukt zu regulieren, und zwar indem die Biosynthese des entsprechenden Proteins gehemmt wird. Mit dieser Technologie wäre es auf einen Schlag möglich, an jedem beliebigen Gen bzw. Protein anzugreifen, und das ist in Modellsystemen und -organismen als wissenschaftliches Werkzeug schon längst Realität. Viele dieser Genziele sind aus verschiedenen Gründen nicht für klassische Arzneistoffe, aber auch nicht für Antikörper verfügbar. Es geht bei unserer Erfindung also nicht nur um einen konkreten Arzneistoff für eine bestimmte Anwendung, sondern um eine Technologie-Plattform. Außerdem könnte diese Technologie in der Zukunft eine maßgeschneiderte Therapie, basierend auf einer individuellen genomischen Analyse z. B. eines Tumors ermöglichen.
uni:view: Ist das im Moment noch alles reine Zukunftsmusik, oder werden solche Wirkstoffe auch heute schon therapeutisch eingesetzt?
Winkler: Das enorme Potenzial macht die Technologie – deren Mechanismen im Grunde seit mehreren Jahrzehnten bekannt ist – natürlich sehr interessant für die Biotech- und Pharmaindustrie. Leider haben aber bislang einige wesentliche Probleme die erfolgreiche Entwicklung und den umfangreichen Einsatz eingeschränkt. Derzeit werden nur zwei Oligonukleotid-Wirkstoffe als Medikament angewendet. Wegen ihrer chemischen Eigenschaften gelangen die Substanzen nämlich nur in einem extrem geringen Ausmaß dorthin, wo sie ihre Wirkung entfalten können, das heißt in die entsprechenden Zellen hinein. Möglichkeiten, das zu verbessern sind daher von ungeheurem Interesse.
uni:view: Gibt es schon konkrete Ideen und Ansätze, um diese Probleme zu lösen?
Winkler: Eine attraktive Möglichkeit besteht darin, andere Moleküle zu verknüpfen, um die Eigenschaften gezielt zu modulieren und so etwa die Zellaufnahme zu verbessern, oder rezeptorgesteuert nur bestimmte Gewebe oder Organe anzugreifen. Wir haben einige solcher potenziellen Arzneistoffe entwickelt und dabei auch eine Methode verwendet, mit der diese und ähnliche Konjugate schneller und effizienter zugänglich sind. Unsere Moleküle hatten in einer ersten Testung in einem in-vitro-Tumormodell einen überraschend guten Effekt und wurden deutlich besser aufgenommen.
uni:view: Gibt es einen starken Konkurrenzdruck, wenn es darum geht, diese Wirkstoffe effizienter zu gestalten?
Winkler: In diesem Bereich gibt es viele Unternehmen und auch akademische ForscherInnen, die jeweils unterschiedliche Ansätze zur Lösung der beschriebenen Problematik anwenden. Neben der Optimierung der chemischen Struktur existieren auch Methoden der Nanotechnologie, also Liposomen und andere partikuläre Systeme. Die Konkurrenz ist also ebenso wie das Interesse groß, und letztlich kann erst nach jahrelangen präklinischen und klinischen Entwicklungen der Wert der einzelnen Ansatzpunkte endgültig beurteilt werden. Man kann davon ausgehen, dass es – im wörtlichen Sinn – kein "Patentrezept" geben wird, um die beschriebenen Hindernisse zur erfolgreichen therapeutischen Anwendung zu lesen. Nur die Kombination mehrerer Ansatzpunkte kann den Erfolg bringen.
MEIN HEUREKA-MOMENT:
In der pharmazeutischen Forschung gibt es meines Erachtens selten einen Geistesblitz bzw. führen andererseits oft die raffiniertesten Ideen nicht zum gewünschten Erfolg. Es handelt sich normalerweise – und auch in diesem Fall war das so – um lange und hartnäckige Arbeit mit kontinuierlichen Entwicklungen. Mehrdad Dirin hat in mehreren Jahren Arbeit im Rahmen seiner Dissertation eine Konjugationsmethode entwickelt und eingesetzt, sowie einige Substanzen hergestellt und getestet. Erst am Ende, nach den positiven Ergebnissen im in-vitro-Modell, war absehbar, dass tatsächlich ein gewisser Fortschritt erzielt wurde. Ein Heureka-Moment stellte sich daher erst ein, als wir die pharmakologischen Daten im Zellkulturmodell gesammelt und ausgewertet hatten.
› zum uni:view Dossier "Heureka!"
uni:view: Wie kam es zum Patentantrag und was waren die besonderen Herausforderungen dabei? Wie geht es nun weiter?
Winkler: Nachdem wir die Ergebnisse gesammelt hatten, musste zunächst entschieden werden, ob sie patentierbar sind. Aufgrund der unzähligen Patente und Veröffentlichungen in diesem Gebiet ist es gar nicht so einfach, etwas Neues im Sinn des Patentrechtes zu entwickeln. Nach einer Empfehlung des austria wirtschaftsservice (aws) hat die Universität entschieden, die Erfindung aufzugreifen und ein Patent einzureichen. Dann konnten wir erfolgreich Mittel vom aws im Rahmen der so genannten Prototypenförderung einreichen, die uns erlauben, weitere Entwicklungen durchzuführen und umfangreichere präklinische Daten zu sammeln. Bei positiven Ergebnissen könnte zukünftig eine weitere Entwicklung mit industriellen Partnern erfolgen.
uni:view: Gehört die Erfindung neuer Wirkstoffe zu den Forschungsschwerpunkten am Department für Pharmazeutische Chemie? Woran wird sonst noch aktuell geforscht?
Winkler: Am Department für Pharmazeutische Chemie wird seit längerem im Bereich der Oligonukleotid-Wirkstoffe, besonders Antisense, siRNA, und miRNA geforscht. Neben der Entwicklung potenzieller Wirkstoffe und auch Trägersystemen zum Drug Targeting werden auch andere Aspekte bearbeitet, etwa die biologischen Grundlagen von siRNA und miRNA und mögliche unerwünschte Effekte. Dabei bestehen internationale Kooperationsprojekte mit akademischen Institutionen und der pharmazeutischen Industrie.
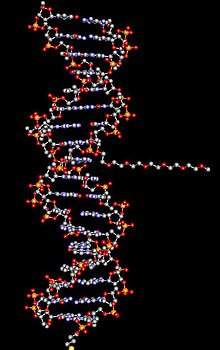
Ein Modell eines der neuen Wirkstoffe: Das computergenerierte Bild zeigt die klassische Struktur eines Nukleinsäureduplexes, an den ein kleines Molekül zur Verbesserung der Aufnahme in Zellen verknüpft ist. (Bild: Mehrdad Dirin) |
|---|
Über Erfindung und Erfinder:
Patenteinreichung "Antisense Oligonucleotides with improved Pharmcokinetic Properties" von Univ.-Prof. i. R. Dr. Christian Noe, Dr. Mehrdad Dirin, Priv.-Doz. Dr. Johannes Winkler, Dr. Bodo Lachmann und Ao.-Univ.-Prof. Dr. Ernst Urban.
Johannes Winkler hat an der Universität Wien Pharmazie studiert. Nach einem Postdoc-Aufenthalt in der Schweiz kehrte er ans Department für Pharmazeutische Chemie zurück und habilitierte sich dort 2014. Der Schwerpunkt seiner Forschungstätigkeit liegt auf der Entwicklung von Oligonukleotiden und passenden Trägersystemen zur therapeutischen Anwendung. Er ist Leiter mehrerer Drittmittelprojekte, darunter ein EU-Verbundprojekt mit Partnern von Universitäten und der Industrie.
Mehrdad Dirin arbeitet als Postdoc am Department für Pharmazeutische Chemie der Universität Wien. Er trat begann sein Doktoratsstudium an der Universität Wien, das er mit der Dissertation "Verbesserung von pharmakokinetischen Eigenschaften der Antisense Oligonukleotide" im Jahr 2012 abschloss. Das Patent beruht hauptsächlich auf Arbeiten im Rahmen seiner Dissertation.
Ernst Urban ist seit 1997 außerordentlicher Professor für Pharmazeutische Chemie an der Universität Wien. Nach dem Studium der Pharmazie und der Promotion 1987 sowie nach Absolvierung eines einjährigen Postdoktorandenaufenthalts an der Universität Heidelberg folgte 1997 die Habilitation für pharmazeutische Chemie. Seine Lehrtätigkeit umfasst Praktika und Vorlesungen aus dem Bereich Pharmazeutische Analytik sowie spezielle Methoden der Pharmazeutischen Chemie und seit 2011 die Lehrbeauftragung mit der Hauptvorlesung aus Pharmazeutische Chemie. Forschungsschwerpunkte sind NMR-Spektroskopie und Strukturaufklärung von Naturstoffen und Syntheseprodukten, Arzneistoffsynthese, Naturstoffsynthese, Reinheitsanalytik von Arzneistoffen, Nukleotide und Oligonukleotide.
Bodo Lachmann ist seit 2008 als "Senior Scientist" am Department für Pharmazeutische Chemie der Universität Wien tätig. Er studierte Pharmazie an der J. W. Gothe Universität Frankfurt am Main, wo auch anschließend seine Promotion begann. Nach Abschluss der Promotion 2000 wechselte er an die Universität Wien, zuerst als Universitätsassistent. Schwerpunkt seiner Arbeiten ist die "Pharmazeutische Analytik" sowie die Qualitätskontrolle von Arzneimitteln.
Christian Noe hat an der Technischen Universität Wien Chemie studiert und 1972 "sub auspiciis" promoviert. Neben seiner Tätigkeit an der TU hat er 1979 auch das Pharmaziestudium an der Universität Wien abgeschlossen. Nach der Habilitation in organischer Chemie 1982 war er ab 1991 C4-Professor an der Universität Frankfurt und ab 1999 Ordinarius für Pharmazeutische Chemie an der Universität Wien, wo er bis zu seinem Ruhestand 2012 das Department für Pharmazeutische Chemie leitete. Er war Dekan an den Universitäten Frankfurt und Wien. Er war Präsident European Federation of Pharmaceutical Sciences (EUFEPS) und Vorsitzender des Scientific Committee der "Innovative Medicines Initiative" (IMI) der Europäischen Kommission. Er ist Ehrenmitglied der Ungarischen Akademie der Wissenschaften. Seine Forschungsinteressen umfassen Nukleinsäure-Therapeutika, Rezeptorantagonisten und -modulatoren (vor allem M3), Stereochemie, Systembiologie, die pathophysiologische Rolle der Blut-Hirn Schranke und translationale Wissenschaften.
Im Dossier "Heureka!" stellt das uni:view Magazin gemeinsam mit der Abteilung Technologietransfer des Forschungsservice der Universität Wien neue Erfindungen der Universität Wien vor. Zum Dossier: "Heureka!"