Mikroskopie per Elektronenstrahl
| 28. Juli 2017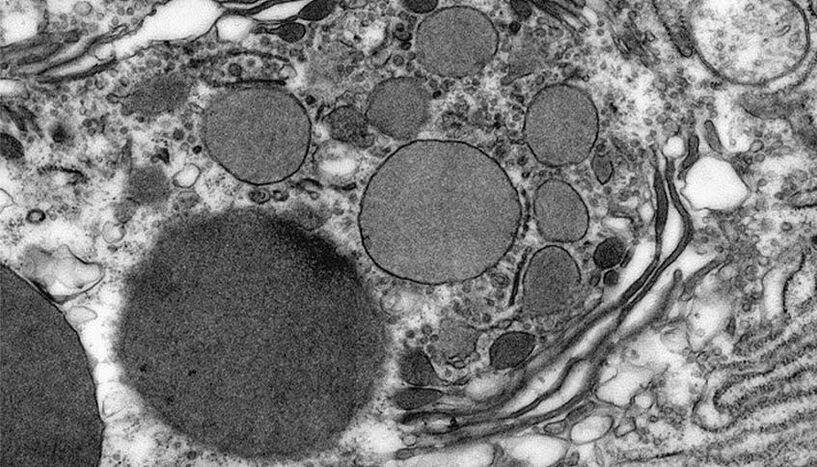
Um derartig detaillierte Aufnahmen von Gewebetypen mit dem Transmissionselektronenmikroskop zu erreichen, ist gute Probenvorbereitung nötig. (Foto: Norbert Cyran)
Die Transmissionselektronenmikroskopie wird seit Jahrzehnten für die biologische Forschung eingesetzt und ist ein unersetzbares Werkzeug, wenn es um Fragen der Zell- und Organell-Morphologie geht.
Praktisch jegliche Art von Gewebe- und Zellproben – von Viren über Bakterien bis zu pflanzlichem und tierischem Material – kann mit den entsprechenden Präparier-Protokollen bearbeitet werden. Diese Präparationen können auf chemischer Fixierung und Prozessierung bei ambienten Temperaturen beruhen, oder aber auf der unmittelbaren Immobilisierung der Lebensprozesse durch schnelles Einfrieren, gefolgt von schneller Dehydrierung und Fixierung bei Kryotemperaturen.
Um optimale Ergebnisse bei der chemischen Präparation unter Raumtemperatur zu erzielen müssen etliche Bedingungen erfüllt sein. So müssen Gewebeproben innerhalb weniger Minuten weiterverarbeitet werden, bevor zellinterne enzymatische Zersetzungsprozesse einsetzen. Entsprechend rasch muss auch die Immobilisierung des Zellinhaltes geschehen, was die Herstellung möglichst kleiner Probenstücke bedingt.
Fixierung von Objekten
Dabei werden das Zytoplasma und die Zell-Organellen durch chemische Querverbindung von Makromolekülen mittels verschiedener Aldehyde im momentanen Zustand 'fixiert'. Zusätzlich werden durch Verwendung von Osmiumtetroxid ungesättigte C=C Verbindungen in den Fettsäuren gesättigt, was im Besonderen alle Membranstrukturen betrifft. Dadurch werden die Zellen auch für den anschließenden Entwässerungsvorgang vor Extraktion durch die verwendeten Lösungsmittel – Alkohol oder Aceton – geschützt. Die Lösungsmittel werden schließlich durch Kunstharz substituiert, das alle ursprünglich wässrigen Komponenten ausfüllt.
Nach dem Polymerisieren des Harzes in Block- oder Kapselform können mit Ultramikrotom und Ultra-Diamantmesser (Abbildung) Ultradünnschnitte (Dicke: 40-80 nm) hergestellt werden. (Foto: Norbert Cyran)
Vor dem Betrachten im Transmissionselektronenmikroskop erfolgt eine Kontrastierung der Schnitte. Dabei werden verschiedene Lantanoiden oder Uranylazetat und Bleicitrat in das Gewebe eingelagert, um den Kontrast von Kohlehydraten, Lipiden und Proteinen zu erhöhen.
Kontrastierung des Ultradünn-Schnittes einer Drüsenzelle
Links: unkontrastierter Schnitt. Rechts: Schnitt nach erfolgter Kontrastierung mit Gadolinium und Bleizitrat. (Fotos: Norbert Cyran)
Immunogold-Markierung von Proteinen
Für die hochauflösende Detektion spezifischer Moleküle können Immunmarkierungen direkt am Ultradünnschnitt gemacht werden. Dabei setzt sich der primäre Antikörper an das Zielmolekül und wird durch den Goldkorn-markierten sekundären Antikörper markiert. Die kugelförmigen Goldkörnchen werden von 1 bis 20 nm Größe angeboten und sind wegen ihrer elektronendichten Struktur am Schnitt relativ gut als tiefschwarze runde Strukturen sichtbar.
Immuno-Gold-Labelling
Links: Antikörper mit Bindungsstelle für das gesuchtes Molekül, markiert mit einem oder mehreren Goldkörnchen im direkten oder indirekten Markierungsverfahren . Rechts: Flagellin-Labelling an einer Bakteriengeißel (J. Montanaro-Punzengruber); einige Goldkörnchen sind durch rote Kreise hervorgehoben. (Fotos: Norbert Cyran)
Elektronen-Energieverlust-Spektroskopie
Das Transmissionselektronenmikroskop kann auch zu analytischen Zwecken verwendet werden, da unser Gerät LIBRA 120 mit einem Energiefilter ausgestattet ist. Strahl-Elektronen haben eine erheblich höhere kinetische Energie als die Elektronen der Atome in der Probe. Wenn sie miteinander wechselwirken, wird ein Schalen-Elektron der Probe auf ein höheres Energieniveau gehoben, während das Strahl-Elektron die für den Quantensprung erforderliche Energie abgibt.
Ein in der TEM-Säule angebrachtes Spektrometer fächert die Elektronen entsprechend ihrer kinetischen Energie auf und erzeugt ein Linien-Intensitätsprofil, aus dem der Photomultiplier das Spektrum berechnet. Die Energiedifferenzen sind element-spezifisch und können für die Elementanalyse herangezogen werden. Mit dem Energiefilter (Spaltblende) können elementspezifische Energiebereiche selektiert und Verteilungsmuster bestimmter Elemente aufgenommen werden.
Elementanalyse mittels Elektronen-Energieverlust-Spektroskopie
Links: Aus dem Linien-Intensitäts-Profil wird das Spektrum kalkuliert, um in der Probe enthaltene Elemente anzuzeigen. Rechts: Die Verwendung des Energiefilters ermöglicht selektive Bildaufnahmen spezifischer Energiebereiche zum Anzeigen des Verteilungsmuster enthaltener Elemente (in blau). (Fotos: Norbert Cyran)
Norbert Cyran ist an der Core Facility für Cell Imaging und Ultrastrukturforschung der Universität Wien tätig.