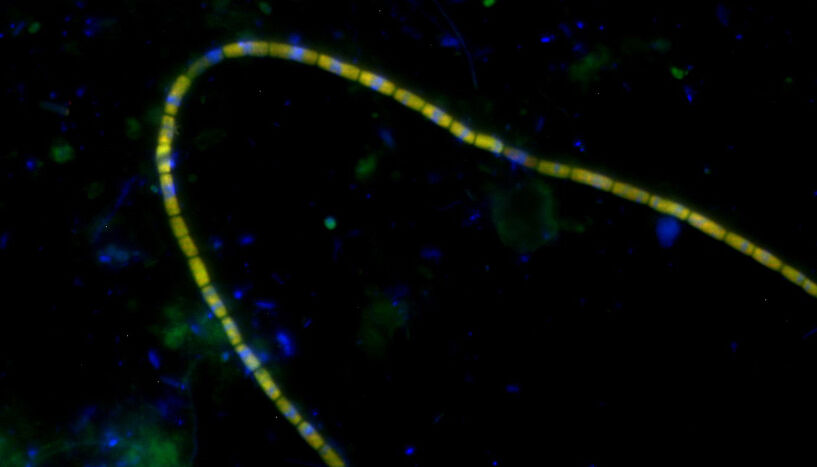
Unerwartete Arbeitsteilung bei Kabelbakterien
20. August 2019Die weltweit vorkommenden Kabelbakterien bilden elektrisch leitfähige, zentimeterlange Filamente. Kabelbakterien oxidieren Sulfid in tieferen, sauerstofffreien Sedimentzonen und leiten die dabei gewonnenen Elektronen zur Sedimentoberfläche, um dort Sauerstoff zu Wasser zu reduzieren. Durch diese ungewöhnliche Fähigkeit zum Elektronentransport über große Distanzen sind Kabelbakterien äußerst erfolgreich und können für einen Großteil des Sauerstoffverbrauchs im Meeresboden verantwortlich sein. Bislang war jedoch nicht bekannt, welche Stoffwechselwege und Enzyme Kabelbakterien für ihren Metabolismus verwenden. Ein internationales Team um Andreas Schramm von der Aarhus University in Dänemark sowie Markus Schmid und Michael Wagner vom Zentrum für Mikrobiologie und Umweltsystemwissenschaft der Universität Wien entwickelte erstmals ein metabolisches Modell der Kabelbakterien. Dabei zeigte sich auch eine unerwartete Arbeitsteilung zwischen Zellen am anodischen und kathodischen Ende der Filamente. Die Studie erscheint aktuell in der Zeitschrift "PNAS".
Stromleitung als Konkurrenzvorteil
Kabelbakterien kommen in riesigen Mengen in den Sedimenten von Gewässern vor. So durchziehen einen Quadratmeter Meeresboden tausende Kilometer von Bakterienkabeln. Die Kabel werden von bestimmten, erst vor wenigen Jahren entdeckten Bakterien gebildet, indem sich zehntausende ihrer Zellen hintereinander reihen und viele Zentimeter lange, elektrisch leitfähige Filamente bilden. Durch diesen Trick können sie – im Gegensatz zu ihren einzelligen Konkurrenten im Sediment – Sulfid als Nahrung nutzen, das in großen Mengen in tiefen, sauerstofffreien Sedimentschichten vorkommt, und die bei der Sulfidoxidation gewonnenen Elektronen nach Leitung durch das Kabel in der sauerstoffreicheren, oberen Sedimentschicht mit Sauerstoff veratmen. Folglich finden die für die Energiekonservierung der Kabelbakterien zentralen Redoxhalbreaktionen (Sulfidoxidaton, Sauerstoffreduktion) nicht wie sonst bei Bakterien üblich in derselben Zelle, sondern in mehreren Zentimetern und vielen tausenden Zellen auseinanderliegenden Bereichen der Kabel statt.
Neue Einblicke mittels Metaproteogenomik und Einzelzellgenomik
Kabelbakterien können im Labor noch nicht in Reinkultur gezüchtet werden und somit waren bislang keine molekularen Details über deren Metabolismus bekannt. "Durch Genomsequenzierung einzelner Kabelbakterienfilamente sowie durch Einsatz metagenomischer Methoden, bei denen die komplexen mikrobiellen Lebensgemeinschaften der Sedimente gemeinsam sequenziert werden, konnten wir nun erstmals die Genome von sechs Kabelbakterien rekonstruieren", berichtet Andreas Schramm, Leiter des aktuellen Forschungsprojekts. "Mittels Metaproteomik testeten wir, welche dieser Gene in den Kabelbakterien tatsächlich exprimiert werden, und konnten somit ein Stoffwechselmodell der Kabelbakterien erstellen".
Überraschenderweise zeigt sich dabei, dass die Kabelbakterien zur Sulfidoxidation einen bereits bekannten Stoffwechselweg, den sulfatreduzierende Bakterien zur Sulfidbildung verwenden, einfach "umgedreht" haben. Dazu passt, dass die Kabelbakterien mit diesen sulfatreduzierenden Bakterien eng verwandt sind.
Wie aber transportieren die Kabelbakterien, die aus der Sulfidoxidation im anodischen Bereich der Kabel gewonnenen Elektronen zum Sauerstoff am kathodischen Ende der Kabel? Hierbei scheint das sogenannte Pilus-Protein PilA eine entscheidende Rolle zu spielen: Es ist das am stärksten exprimierte Protein in der Proteomanalyse und könnte zu elektronenleitenden Fasern an der Außenseite der Kabelbakterienfilamente aggregieren.
Unerwartetes Abfackeln der Elektronen am kathodischen Ende
Die meisten atmenden Lebewesen nützen die Reduktion von Sauerstoff zu Wasser zur Energiekonservierung. Hierfür sind sogenannte terminale Oxidasen notwendig, die als Proteinkomplexe in der Membran vorkommen. Völlig überraschend konnten in den Genomen der Kabelbakterien keine entsprechenden Gene gefunden werden. Vielmehr scheinen die Kabelbakterien an der kathodischen Seite ihrer Filamente die Elektronen aus der Sulfidoxidation ohne Energiekonservierung zur Sauerstoffreduktion zu verwenden. Vermutlich ist diese Energieverschwendung notwendig, um schnell genug Elektronen auf Sauerstoff übertragen zu können. Ein Großteil der Zellen in den Filamenten ist in sauerstofffreien, sulfidhaltigen Zonen angesiedelt und nur wenige Zellen an einem Ende der Filamente reichen in den oberen Bereich der Sedimente, in dem Sauerstoff enthalten ist.
Folglich können viel mehr Zellen Elektronen mittels Sulfidoxidation freisetzen als mittels Sauerstoffreduktion verbrauchen. Somit müssen die sauerstoffreduzierenden Zellen bis zu zehnmal schneller arbeiten, was nur unter Verzicht auf Energiekonservierung in diesen Zellen möglich zu sein scheint. In den Kabelbakterien herrscht also eine strikte Arbeitsteilung zwischen den Zellen am anodischen und kathodischen Ende, wobei die Zellen am kathodischen Ende keine Energie konservieren und nur durch Reservestoffe für eine kurze Zeit überleben können und ein hohes Absterberisiko haben. Passend zu dieser Theorie konnte in der Studie experimentell nachgewiesen werden, dass Kabelbakterien den Großteil ihrer Proteine im anodischen Bereich synthetisieren.
Kabelbakterien können sich schnell und schlängelnd fortbewegen und dabei auch gezielt in sauerstoffhaltige Bereiche vordringen, während ein Großteil der Kabel in sauerstofffreien Bereichen verbleibt. Dabei werden die Zellen in der sauerstoffhaltigen Zone kurzzeitig als Kathode verwendet, um Elektronen abzufackeln, bevor sie wieder in sauerstofffreie Bereiche gezogen werden und andere Zellen ihre Aufgabe als Elektronensenke erfüllen.
"Das erarbeitete Stoffwechselmodell der Kabelbakterien enthält viele große Überraschungen. Im nächsten Schritt müssen diese nun unbedingt experimentell überprüft werden", erläutert Michael Wagner, Leiter des Zentrums für Mikrobiologie und Umweltsystemforschung an der Universität Wien. "Hierzu gehört auch die Frage, ob die Kabelbakterien neben Sauerstoff auch, wie aus den Genomanalysen angezeigt, Nitrit und Nitrat als alternative Elektronenakzeptoren nutzen und welche ökologischen Konsequenzen aus dieser zusätzliche metabolischen Flexibilität erwachsen würden".
Publikation in PNAS: Kasper U. Kjeldsen, Lars Schreiber, Casper A. Thorup, Thomas Boesen, Jesper T. Bjerg, Tingting Yang, Morten S. Dueholm, Steffen Larsen, Nils Risgaard-Petersen, Marta Nierychlo, Markus Schmid, Andreas Bøggild, Jack van de Vossenberg, Jeanine S. Geelhoed, Filip J. R. Meysman, Michael Wagner, Per H. Nielsen, Lars Peter Nielsen, and Andreas Schramm: On the evolution and physiology of cable bacteria.
Rückfragehinweis
Mag. Alexandra Frey
Media Relations ManagerUniversität Wien
1010 - Wien, Universitätsring 1
+43-1-4277-17533
+43-664-8175675
alexandra.frey@univie.ac.at
Downloads:
Wagner_Kabelbakterien_1.jpg
Dateigröße: 197,74 KB
Wagner_Kabelbakterien_2.jpg
Dateigröße: 246,17 KB